Nell’esperimento di Miller, quello delle scariche elettriche sopra il liquido simulante il cosiddetto ‘brodo primordiale’, si formano solo tredici dei venti amminoacidi necessari, ma se ne sintetizzano anche tanti altri che non compaiono negli esseri viventi: non si riesce perciò a spiegare come mai nella costruzione delle proteine ne siano presenti solamente alcuni, pur essendo la scelta disponibile molto più ampia, e non si capisce da dove siano saltati fuori i rimanenti altri sette che non vengono sintetizzati in tale brodo. Anzi in quest’ultimo, fra l’altro, abbondano le cosiddette molecole ‘monofunzionali’, che ostacolano la formazione di lunghe catene e quindi in definitiva impediscono la formazione delle proteine stesse.
Ogni amminoacido ha come un uncino (chiamato gruppo amminico) e un anello (detto gruppo carbossilico) che si agganciano in sequenza rispettivamente ad un amminoacido precedente e ad uno successivo della catena, così come si legano i vagoni di un treno, ma in questo vincolamento, che viene chiamato condensazione, si produce una molecola di acqua come residuo. Il processo inverso detto idrolisi, cioè diluizione in acqua, e che porta allo sganciamento degli amminoacidi con la distruzione della catena, è più probabile, quindi l’acqua non favorisce la formazione delle catene, semmai la ostacola. E i brodi primordiali erano costituiti in massima parte di acqua. Sono state fatte allora anche altre ipotesi di esistenza di sistemi non acquosi, ma sussiste sempre il problema che durante le reazioni di condensazione l’acqua prodotta deve essere continuamente eliminata se non si vuole che il processo si arresti.
Per dirla con Junker e Scherer perciò “gli esperimenti di Miller (…) portano ad un vicolo cieco, visto che in tutti gli approcci sperimentali, oltre agli amminoacidi desiderati (e non tutti quelli necessari - nota mia) si forma un gran numero di altre sostanze che impediscono i passi successivi. Tutti gli studi sui passi successivi (cioè su quelli che servono per costruire le proteine – nota mia) partono da miscugli ‘puri’ di amminoacidi non ottenuti in ambiente abiotico. Ciò significa che i complessi problemi di sintesi, isolamento e purificazione vengono dati per risolti, senza però essere stati affrontati nella discussione” (1)
Le proteine, che costituiscono la struttura dell’essere vivente e svolgono le funzioni vitali, sono formate con una sequenza apparentemente casuale degli amminoacidi scelti tra i 20 ‘vitali’. Ci sono proteine che sono composte anche da una catena di migliaia di amminoacidi con un ordine ben preciso e immutabile, e tipico della proteina stessa, tanto che basta scambiare di posto due degli anelli che formano la sequenza, o sostituirne uno con un altro, per sovente rovinarle (come succede ad esempio nell’emoglobina, in cui la sostituzione con un altro di uno solo tra i 600 amminoacidi che la compongono provoca l’anemia falciforme). Insomma, l'ordine di assemblaggio è fondamentale quanto quello delle lettere dell'alfabeto nella composizione delle parole.
Le proteine hanno una forma iniziale lineare e sono in pratica come delle frasi in cui le lettere sono gli amminoacidi. Possono essere sia strutturali, come pezzi che costituiscono fisicamente un macchinario, sia funzionali, cioè che svolgono una funzione, un compito ben determinato, come ad esempio fanno gli enzimi, e che quindi in definitiva posseggono ‘informazione’. Supporne la formazione casuale, sarebbe equivalente ad ipotizzare che si siano formate spontaneamente delle frasi ‘sensate e operative’ e alcune tanto lunghe che potrebbero riempire diverse pagine di un libro.
Ma non finisce qui. Moltissime proteine devono anche assumere una particolare forma spaziale per poter funzionare. Ci sono ben quattro di queste disposizioni, ognuna seguente l’altra e sempre più complessa: quella lineare che è la più semplice, l’altra a elica detta struttura secondaria, l’altra ancora con l’elica ripiegata su se stessa detta struttura globulare e la quarta, come l’emoglobina, in cui più avvolgimenti globulari si legano tra loro e cooperano.
Insomma, come dice Guerra, “le difficoltà salgono alle stelle, quando si prende in considerazione la seconda fase dell’«evoluzione chimica», durante la quale le «molecole prebiotiche» avrebbero reagito fra loro per formare polisaccaridi, polipeptidi – e poi proteine – e polinucleotidi – e poi acidi nucleici –, che unendosi insieme avrebbero formato i primi organismi. Qui il «caso» invocato dagli abiogenisti si rivela molto intelligente” (2).
L'organismo più semplice (il batterio escherichia coli) ha circa 600 proteine di diverso tipo e l'uomo ne ha 10.000, ognuna con un compito funzionale o strutturale ben preciso.
Ma qual’è la probabilità di formazione casuale di una proteina funzionante?
La domanda che ci poniamo è: ‘quale dev’essere la struttura di una proteina perché possa svolgere una funzione biologica? Quante sequenze (di aminoacidi) possono svolgere una stessa determinata funzione?’ (3).
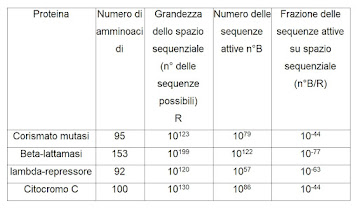
Supponiamo di voler considerare una proteina molto semplice, composta ad esempio da 100 amminoacidi scelti tra i 20 utilizzabili. Le possibili combinazioni differenti sono 20100 ( ) che è circa uguale a 10130 (cioè 1 seguito da 130 zeri…) e se consideriamo che il numero stimato di particelle subatomiche che compongono l’intero Universo è di 1084 si può avere una certa idea di quanto grande possa essere questo numero, una grandezza ‘transastronomica’. Tale numero viene detto ‘spazio sequenziale R’ della proteina considerata, esso indica in definitiva tutte le possibili proteine composte da una sequenza di 100 amminoacidi (perciò R = insieme delle 'proteine' composte da 100 amminoacidi). Tra queste solo alcune sono avvolte in maniera stabile, quindi solo un sottoinsieme F di R di 100 amminoacidi (F = insieme delle proteine di 100 amminoacidi e stabili ) e tra queste solo poche hanno un’attività biologica, quindi quelle appartenenti ad un ulteriore sottoinsieme di F indicato con A (A = insieme delle proteine di 100 amminoacidi, stabili e con attività biologica). Fissata una data funzione che la proteina deve svolgere, bisogna però tenere presente che in A ci sono diverse combinazioni che danno la stessa funzione e chiameremo B questo sottoinsieme di A (B = insieme delle proteine di 100 amminoacidi, stabili, con attività biologica e che svolgono la stessa fissata funzione) (e il suo numero n°B si chiama ‘numero delle sequenze attive’ relativo a quella funzione). Al presente si è in grado di fare delle stime almeno approssimative sul numero di sequenze attive n°B che, in un determinato spazio sequenziale R, sono capaci di svolgere la stessa fissata funzione e ne riporto alcune nella seguente tabella tratta dal libro di Junker-Scherer (4):
Che significato ha questa tabella? Il dato importante per ogni proteina è quello espresso dall’ultima colonna: tale numero dà la probabilità del suo formarsi casuale. Come si vede sono numeri molto bassi, quasi nulli. Ad esempio la probabilità di formarsi della Beta-lattamasi, o di un'enzima che ha la stessa sua funzione, è dello 0,….1% dove i puntini intermedi indicano la presenza di altri 74 zeri! Si potrebbe obietterare che il materiale a disposizione sulla Terra è molto grande e quindi con le combinazioni casuali possibili la probabilità è immensamente più grande. Ma se si procede anche ad un calcolo ottimistico ed estremo è comunque "estremamente improbabile che una proteina funzionale venga prodotta tramite un processo casuale in un brodo primordiale. IL carbonio contenuto nella biomassa della Terra è di circa 280 miliardi di tonnellate, utilizzandolo tutto per produrre, ad esempio proteine con 153 amminoacidi, risulta che la probabilità matematica che tra esse si trovi una Beta-lattamasi sarebbe 10-77 x 1037 = 10-44 (ovvero lo 0,...1 % con al posto dei puntini 41 zeri! - nota mia)" (5)
Fra l'altro nei tentativi di costruzioni casuali fatti in laboratorio, non è risultato neanche per sbaglio un caso positivo:“sono state prodotte in laboratorio sequenze casuali di amminoacidi tramite processi di ingegneria genetica; il numero di sequenze differenti che possono essere prodotte in un esperimento è al massimo di 1014 varianti. Finora non si è riuscito a trovare neppure una sequenza con una struttura spaziale stabile o che addirittura presenti un’attività enzimatica” (5).
A
dire il vero però gli evoluzionisti non affermano che le moderne
proteine siano spuntate così come sono nelle cellule primitive, ma
suppongono che quelle contenute in quelle protocellule fossero molto
semplici e che a partire da una loro funzione primitiva si sia giunti alla
complessità attuale tramite innumerevoli passi microevolutivi di
ottimizzazione. Ma come si è visto, una seppur minima variazione nella struttura di una proteina ha come conseguenza solitamente la perdita della sua funzione se non addirittura la sua dannosità!
Quindi una variazione avrebbe portato, almeno nella stragrande maggioranza dei casi, ad uno svantaggio 'evolutivo' e non ad un vantaggio, e sarebbe stata eliminata dalla selezione. Ma anche ammesso che delle variazioni potessero conservarsi, per ottenere le complesse proteine attuali, con centinaia e migliaia di amminoacidi, queste proteine, supposte inizialmente semplici, con l'ulteriore addizione casuale di altri amminoacidi si sarebbero dovute avventurare per ogni aggiunta in 'spazi sequenziali' sempre più vasti e azzeccare quindi una forma 'utile' sempre meno probabile. Quindi questo supposto processo evolutivo, che a partire da una proteina semplice con piccole mutazioni casuali avrebbe portato a quelle più complesse, appare poco realistico, e perciò ben lungi da essere plausibile, anzi irragionevole. E comunque anche questo evento non è neanche lontanamente provato sperimentalmente, come d'altronde non lo sono molte altre numerose supposizioni e affermazioni della teoria evolutiva.
Ma fra l’altro quanto potrebbe essere semplice una proteina attiva? Ad esempio un enzima? Innanzitutto bisogna vedere quale può essere il numero minimo di amminoacidi, scelti tra i 20, che ne faccia ottenere una funzionale. Nelle ricerche effettuate le proteine con meno di 9 tipi diversi di amminoacidi non presentano alcuna azione enzimatica. E quanto deve essere minimo lunga una catena di amminoacidi per poter svolgere una funzione biologica ed essere stabile? Non entro nei dettagli, ma si è trovato che non può essere inferiore a 50 (6). Quindi, supposto che la proteina primitiva fosse formata con solo 9 tipi di amminoacidi e fosse lunga 50, risulta uno spazio sequenziale R di 950 cioè circa 5x1047 varianti, in effetti molto inferiori rispetto a quelli indicati nella seconda colonna della tabella. Ma quale frazione di questo numero si deve ipotizzare come realisticamente formato da proteine stabili e funzionali? Ancora non sono stati fatti esperimenti per scoprirlo, ma si presume che tale numero sia molto inferiore a quello delle complesse proteine attuali (e quindi con una probabilità di formazione spontanea più piccola): infatti la capacità di avvolgimento (essenziale per le proteine) viene destabilizzata dalla minore lunghezza. E allora in conclusione tutto ciò fa dire a Junker e Scherer, “nel complesso quindi ci sono dei motivi per pensare che una riduzione dell’alfabeto degli amminoacidi e una riduzione della lunghezza delle sequenze di proteine ipotetiche non portino alla soluzione del problema della formazione (spontanea) delle proteine necessarie alla vita di una prima cellula” (7).
Ma i problemi non finiscono qui. Infatti questo discorso riguarda il formarsi casuale di un solo tipo di proteina, ma ovviamente una cellula non può funzionare con un solo tipo di essa, ne occorrono di diverse, con funzioni differenti, e quindi si deve supporne il formarsi spontaneo di altre, anche se magari più semplici di quelle attuali. Ma allora bisogna ulteriormente chiedersi: qual’è il numero minimo di proteine diverse con cui una cellula primitiva avrebbe potuto funzionare?
(continua)
______________________________________
Note e crediti
(1) Junker e Scherer – Evoluzione – un trattato critico – Gribaudi 2007– pag. 104
(2) Giulio Dante Guerra – L’Origine della vita – il ‘caso’ non spiega la realtà – D’Ettoris Editori 2015 – pag. 16
(3) Junker e Scherer – op.cit. Pag. 125
(4) Junker e Scherer – op. cit. pag. 126
(5) Junker e Scherer – op. cit. pag. 127
(6) vedi Junker e Scherer – op. cit. pag 127
(7) Junker e Scherer – op. cit. pag 128

Grazie per le tue analisi come questa, molto interessanti.
RispondiEliminaD.N. Il professor Canto parla di sequenze attive di aminoacidi: queste proteine attive sono in sostanza gli enzimi. Accenna pure alla forma tridimensionale che assumono le sequenze di aminoacidi, forma tridimensionale che è strettamente collegata alla funzione di tutte le proteine e in particolare alla funzione di ciascun enzima.
RispondiEliminaA chi volesse addentrarsi un poco in questo mondo, e capire che cosa si intenda per attività di un enzima, suggerisco di dedicare un quarto d'ora a un enzima "spettacolare" la cui struttura e il cui funzionamento sono stati chiariti e divulgati. Dico divulgati perché chi vuole può trovare dei video interessanti su questo enzima anche su youtube.
L'enzima si chiama ATP SINTETASI e conclude per così dire la serie di reazioni che rendono disponibile alla cellula l'energia contenuta negli zuccheri, dai quali tutta una batteria di precedenti enzimi ha provveduto a staccare gli atomi di idrogeno che fanno funzionare l'ATP SINTETASI.
C'è nei video su youtube il problema della lingua (sono in inglese), ma le animazioni sono ben fatte e danno l'idea visiva di come funziona questo enzima. In poche parole, anche il profano può farsi un'idea di come funzioni una "macchina molecolare", senza però dimenticare che quello che vede a colori in realtà non è colorato e ha dimensioni dell'ordine dei milionesimi di millimetro.
Spero di avere dato uno spunto per chi fosse interessato a capire qualcosa di più su che cosa si intenda per attività di un enzima,